Sygeplejersken
Nye resistente bakterier forebygges med gamle metoder
Antibiotikaforbruget og ikke mindst valget af antibiotika spiller en central rolle for resistensudviklingen, som er blevet et stigende sundhedsproblem. Artiklen beskriver udviklingen af resistente bakterier og forebyggelse af spredning af disse bakterier. Artiklen har fokus på de infektionshygiejniske forebyggende foranstaltninger, som beskrives i nationale infektionshygiejniske vejledninger. Artiklen er fagfællebedømt.
Sygeplejersken 2011 nr. 20, s. 63-69
Af:
Anne Kjerulf, afdelingslæge, ph.d.,
Jette Holt, hygiejnesygeplejerske, cand.pæd.pæd.

- At beskrive udviklingen af specifikke resistente bakterier.
- At gøre rede for forebyggelse af spredning af disse bakterier.
- At skærpe fokus på hygiejne både i den primære og i den
sekundære sundhedssektor.
Den største trussel mod folkesundheden var indtil for ca. 50 år siden infektionssygdomme, som forårsagede sygdom hos i forvejen raske og sunde mennesker, ofte børn og unge. Infektionssygdomme havde en betydelig dødelighed og optrådte ofte i epidemier, som f.eks. mæslingeepidemier.
Anvendelse af antibiotika og indførelse af obligatoriske børnevaccinationer samt ikke mindst en forstærket indsats på det infektionshygiejniske område i form af udarbejdelse og implementering af vejledninger om hygiejne har kunnet holde antallet af ikke blot sundhedssektorerhvervede, men også samfundserhvervede infektionssygdomme på et lavt niveau i Danmark.
En restriktiv antibiotikapolitik med hovedvægt på anvendelse af smalspektrede antibiotika har hidtil kunnet fastholde antallet af resistente bakterier på et meget lavt niveau, så antibiotikabehandling af patienten har været mulig. Denne æra ser desværre ud til at være forbi nu. Hvordan opstår resistens?
Alle mikroorganismer, bakterier, virus og svampe kan udvikle resistens, dvs. blive modstandsdygtige over for de antimikrobielle midler, som vi i dag anvender til behandling af infektioner (1). Udvikling af antibiotikaresistens fremmes såvel af et øget forbrug som af en uhensigtsmæssig anvendelse af bredspektrede antibiotika. Antibiotika slår de følsomme bakterier ihjel, mens de resistente bakterier bliver tilbage og vokser frem i større mængder, når konkurrencen fra de følsomme bakterier er forsvundet (selektion).
Når antibiotikapåvirkningen ophører, vender de følsomme bakterier tilbage og udkonkurrerer de resistente igen. Derfor skal antibiotika kun bruges, når sygdomsfremkaldende bakterier skal fjernes, så selektion/udvælgelse af resistente bakterier undgås. Antibiotikaforbruget og ikke mindst valget af antibiotika spiller en central rolle for resistensudviklingen, som er blevet et stigende sundhedsproblem.
Det er her vigtigt at huske, at ved mistanke om infektion skal der tages mikrobiologiske prøver, inden man påbegynder behandling med antibiotika. Når svar på prøverne foreligger, skal behandlingen justeres efter disse, så patienten får den mest optimale antibiotikabehandling. Gennem de seneste 10-15 år har resistensudviklingen overhalet produktionen af nye antibiotika, som er effektive mod resistente bakterier.
Der findes derfor nu sygdomsfremkaldende bakterier, hvor man ikke har et antibiotikum, som man kan behandle patientens infektion med (1). Forklaringerne på den øgede resistensudvikling i Danmark er dels et øget forbrug af antibiotika til såvel mennesker som dyr de senere år, dels at der i stigende grad anvendes bredspektrede antibiotika frem for smalspektrede (2,3).
Ifølge den seneste Danmap-rapport fra 2010 har der været en stigning i det samlede antibiotikaforbrug til mennesker fra 2001 til 2010 på 32 pct., og fra 2009 til 2010 sås en stigning på 5 pct., hvilket skyldes et øget forbrug i primærsektoren (3). Antibiotikaforbruget til produktionsdyr er derimod faldet med 3 pct. fra 2009 til 2010 efter indførelse af en såkaldt ”gul kort”-ordning og landbrugets frivillige stop for brug af bredspektrede antibiotika herunder især cefalosporiner pr. 1. juli 2010.
Denne ordning har været en succes, da forbruget af disse bredspektrede antibiotika er faldet med 47 pct. for svin og 35 pct. for kvæg (3). Det totale forbrug af bredspektrede antibiotika til mennesker er derimod steget med 7 pct. fra 2009 til 2010 (3). På internationalt plan har denne resistensudvikling stået på i længere tid (4). Indtil for ganske få år siden blev hovedparten af resistente bakterier således importeret til det danske sundhedsvæsen via patienter, der havde været indlagt på udenlandske hospitaler.
Resistente bakterier i Danmark
I de senere år har vi i Danmark set en øget forekomst af især modstandsdygtige stafylokokker (MRSA, resistente tarmbakterier (f.eks. ESBL-producerende E. coli og Klebsiella) og virulente stammer af tarmbakterien Clostridium difficile (f.eks. 027) i form af såvel enkeltstående tilfælde som større og mindre udbrud.
Hvor man tidligere kun så disse resistente bakterier på hospitalerne, så har man de senere år også fundet disse i stadigt større antal i primærsektoren (5). Frem til år 2003 var der en lav forekomst af MRSA i Danmark på ca. 100 tilfælde pr. år, men fra 2003 sås en markant stigning (6).
Efter at MRSA blev en anmeldelsespligtig sygdom i 2006, og infektionshygiejniske retningslinjer for MRSA blev implementeret på danske hospitaler og i primærsektoren (7), er der set et fald i forekomsten af hospitalserhvervede MRSA-tilfælde (bærertilstand/ infektion), men en stigning i antallet af samfundserhvervede tilfælde, som her dækker samfundet og primærsektoren.
I 2010 var der således 1.097 nye MRSA-tilfælde (en stigning på 34 pct. i forhold til 2009), hvoraf 578 var samfundserhvervede, og kun 62 var hospitalserhvervede (3). Siden januar 2009 har der været flere større udbrud med C. difficile 027 på danske hospitaler, særligt på Sjælland (8,9). I marts 2009 blev der iværksat en national laboratorieovervågning af C. difficile 027 (8), og i 2010 var der i alt 856 patienter med denne diagnose, hvilket er en stigning på 44 pct. i forhold til 2009 (8).
Der er ingen national laboratorieovervågning af ESBL-producerende bakterier i Danmark, men der er foretaget to prævalensundersøgelser i 2007 og 2009, der viste, at forekomsten af ESBLproducerende Klebsiella pneumonia og E. coli er steget markant inden for kun to år (10,11).
Prævalensen af ESBL-producerende K. pneumoniae i bloddyrkninger steg således fra 5 pct. i 2007 til 14,6 pct. i 2009, de tilsvarende tal for ESBL-producerende E. coli var 4,2 pct. i 2007, der steg til 7 pct. i 2009. Da forekomsten af patienter med ESBL-resistente bakterier er langt højere end patienter med MRSA i Danmark, er dette et meget alvorligt problem, der kræver snarlig handling.
De resistente bakterier kan give svære infektioner, som er vanskelige at behandle, men er desuden også forbundet med øget sygelighed og dødelighed, længere indlæggelsestid og dermed større omkostninger såvel for patienten som for samfundet. Resistente bakterier kan også blot kolonisere personen, som således ingen symptomer får, men derimod status som rask smittebærer.
At være koloniseret betyder, at man bliver bærer af bakterierne på huden, slimhinderne (især næse og svælg), i huddefekter eller i tarmen afhængigt af, hvilken bakterie det drejer sig om. MRSA kan kolonisere hud og slimhinder, og ESBL-producerende bakterier og C. difficile 027 koloniserer tarmen.
En bærertilstand er en risikofaktor for senere udvikling af en infektion hos bæreren, f.eks. i forbindelse med en antibiotikabehandling med et bredspektret antibiotikum, men en bærer kan også sprede bakterien til andre og til miljøet gennem hudskæl, berøring eller ved toiletbesøg. Indlæggelse eller arbejde i sundhedssektorer uden for Norden er en risikofaktor for at blive koloniseret med MRSA, men MRSA er gennem de senere år i stigende grad set som smitte erhvervet i samfundet ved social kontakt (6,7).
Svin får bredspektret antibiotika
Grunden til, at vi i dag ser smitte med resistente bakterier, herunder især ESBL-producerende tarmbakterier, er et stadigt stigende forbrug af bredspektrede antibiotika, ikke blot til mennesker, men også til produktionsdyr (især svin) i landbruget såvel nationalt som internationalt. Ifølge danske undersøgelser har 11 pct. af danske svin ESBL-producerende bakterier i deres tarm, og forekomsten af disse bakterier er endnu højere i importerede fødevarer, f.eks. 36 pct. i importeret fjerkrækød (11).
Raske smittebærere kan således have erhvervet de resistente bakterier gennem social eller professionel kontakt eller gennem forurenede fødevarer. Svenske undersøgelser har vist, at mellem 24-36 pct. af ferierejsende uden for Europa var bærere af ESBLproducerende bakterier i deres tarm, uden på nogen måde at have været i kontakt med sundhedsvæsenet (12,13).
Ved rejser til Ægypten, Mellemøsten, Indien og Asien var der en markant højere hyppighed af bærertilstand (38-79 pct. (12)).
- Hvor hyppigt diskuterer I de generelle infektionshygiejniske retningslinjer på jeres arbejdsplads?
- Tilrettelægger I jeres arbejdsprocedurer anderledes, hvis I ved, at I har en patient med en smitsom sygdom?
- Er værnemidler (f.eks. handsker, maske, briller, forklæde) lettilgængelige på arbejdspladsen?
- Hvilke ressourcepersoner trækker I på, hvis I er i tvivl om hygiejnen i en specifik situation på jeres arbejdsplads?
Raske smittebærere udgør en risiko
Infektionsproblematikken er således væsentligt ændret i dag, vi kan ikke nødvendigvis vaccinere eller behandle os ud af infektionerne mere.
Det er ikke kun på hospitalerne, resistensproblematikken eksisterer, men også i primærsektoren, og smitterisikoen eksisterer ikke kun hos de synligt syge, men også hos raske smittebærere. Bærertilstanden i primærsektoren og samfundet udgør således ikke kun en risiko for den raske smittebærer i tilfælde af, at han bliver syg, men også for resten af samfundet, idet bakterien spredes videre ind i sundhedsvæsenets institutioner af raske smittebærere.
En invasiv infektion med resistente eller virulente mikroorganismer kræver øjeblikkelig og korrekt behandling. Bærertilstanden kan være langvarig (sjældent livsvarig, dvs. det er muligt at smide bakterierne igen) det er ikke altid muligt at fjerne bærertilstanden, men den er ikke truende for patientens helbred, medmindre bakterierne får mulighed for at invadere organismen og give en infektion.
En bærertilstand med resistente bakterier kan få andre konsekvenser end en bærertilstand med ikke-resistente bakterier, da den mikrobiologiske diagnostik tager længere tid med en forsinkelse i relevant antibiotikabehandling til følge. På mange måder ligner den nuværende situation med resistente bakterier således tiden før opdagelsen af antibiotika.
Behandling dengang var ikke mulig, og der var dermed udelukkende fokus på metoder til forebyggelse af spredning af bakterier. Metoderne til dette var overholdelse af en korrekt hygiejne i form af håndhygiejne, rengøring, desinfektion og sterilisation. Det er således de gamle veldokumenterede infektionshygiejniske dyder, vi igen i dag skal have på banen, nu hvor vi ikke medicinsk kan behandle os ud af smittespredning.
Forebyggelse af spredning af resistente mikroorganismer
Det er i denne sammenhæng vigtigt at huske på, at resistente bakterier spredes på samme måde som ikke-resistente bakterier. Forebyggelse af smittespredning har primært fokus på smitte fra patient til personale, fra personale til patient, men også på smitte fra patient til patient og fra personale til personale. For at en person kan blive koloniseret eller inficeret, skal mange betingelser være opfyldt:
- Mikroorganismen skal være til stede
- Den skal kunne overleve på hænder og i miljøet
- Den skal kunne tåle at blive overført
- De infektionshygiejniske retningslinjer er ikke tilstrækkelige eller bliver ikke overholdt
- Mikroorganismen skal have evnen til at kunne kolonisere eller invadere organismen og forårsage en infektion.
- De bakterier, som man ser giver størst problemer i sundhedsvæsenet, er bakterier, som opfylder alle disse kriterier i særlig høj grad.
Infektionshygiejniske forholdsregler
Infektionshygiejne og især håndhygiejne er veldokumenterede metoder til at forebygge smittespredning både på hospitaler og i primærsektor. Metoderne skal være rettet mod såvel miljøet som personens adfærd i miljøet. Fokus er dermed primært rettet mod smittevejene kontaktsmitte, dråbesmitte og for ESBL og C. difficile’s vedkommende især fækal-oral smitte.
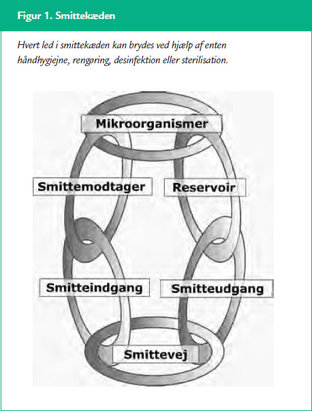
De infektionshygiejniske metoder retter sig både mod at forebygge dannelse af et reservoir for bakterierne i miljøet og på udstyr i form af rengøring, desinfektion og sterilisation og mod smittespredning via hænder i form af håndhygiejne (14,15) (se figur 1 her på siden). Infektionshygiejniske retningslinjer ændrer sig som alle andre retningslinjer, når ny viden eller nye sygdomme erkendes.
I 1992 overgik man således internationalt til ikke længere at arbejde ud fra patientens kendte diagnose og dermed smittestatus, men til at se på de arbejdsprocedurer, hvor personalet kunne komme i kontakt med organisk materiale, der kunne indeholde smitsomme patogene mikroorganismer.
Paradigmeskiftet skyldtes opdagelsen af hiv-infektioner. Denne sygdom gav ikke kendte infektionstegn, infektionen kunne være uerkendt af personen selv, og det var ikke muligt i sygdommens første måneder at se en ændring i blodmarkørerne for de hvide blodlegemer. De diagnoserelaterede retningslinjer for smitte kunne dermed ikke anvendes, og man udarbejdede derfor de procedurerelaterede hygiejniske retningslinjer.
Dette betyder i praksis, at alle patienter skal betragtes som potentielle smittebærere. Dermed undgik sundhedspersonalet også at stigmatisere den smittede patient, idet man nu skulle anvende de samme hygiejniske forholdsregler ved kontakt med alle patienter uanset diagnose (16).
Generelle infektionshygiejniske retningslinjer
I daglig tale kaldes de procedurerelaterede retningslinjer for generelle infektionshygiejniske retningslinjer. De er i dag indarbejdede i alle procedurer i sundhedsvæsenet, hvor risiko for stik- og skæreuheld, stænk og sprøjt eller kontakt med organisk materiale, der kan indeholde patogene mikroorganismer, kan forekomme.
Retningslinjerne gælder dermed for alle patienter og alle personalegrupper med patientkontakt såvel i primærsektor som på hospitalerne (16). Forebyggelse af smitte sker gennem en individuel planlægning og tilrettelæggelse af pleje- eller behandlingsopgaver, så kontakten med organisk materiale undgås. Herefter vælges brug af værnemidler afhængigt af smittevejen.
Anvendelse af værnemidler som handsker, forklæde, briller og maske beskytter således hud, slimhinder og arbejdsdragt mod forurening med sekret, ekskret og blod. Handsker og forklæde beskytter mod kontaktsmitte. Briller og masker beskytter hud og slimhinder mod dråbesmitte i form af stænk og sprøjt med organisk materiale (16).
Supplerende infektionshygiejniske retningslinjer
Hvis de generelle infektionshygiejniske retningslinjer ikke er tilstrækkelige til at forebygge smitte til omgivelser eller andre patienter, må man i tillæg anvende supplerende infektionshygiejniske retningslinjer. Disse anvendes ved dråbesmitte, luftbåren smitte og ved visse infektionssygdomme, som smitter ved kontakt, men som ikke kan forebygges ved anvendelse af de generelle hygiejniske retningslinjer alene.
De supplerende retningslinjer indebærer fysisk isolation af patienten, langærmede overtrækskitler, handsker og evt. maske og briller. Isolation kan desuden indebære særlige rengørings- og desinfektionsprocedurer af kontaktpunkter og overflader på stuen afhængigt af den enkelte mikroorganismes evne til at overleve i miljøet.
Det er veldokumenteret, at isolation kan have psykiske og fysiske konsekvenser i form af depression, forladthedsfølelse og utilsigtede hændelser. En isolation er en lægeordination, der skal dokumenteres i patientens journal, og den skal revurderes med fastlagte intervaller (17). MRSA, Clostridium difficile og ESBL-producerende bakterier (f.eks. Klebsiella, E. coli) smitter ved kontakt med organisk materiale, der indeholder bakterier, dvs. via kontakt med f.eks. fæces, urin, sårsekret og for MRSA’s vedkommende også ved almindelig hudkontakt.
Smittevejen sker således via hænder, udstyr og omgivelser, der berøres af hænder. Hvis mikroorganismerne findes i luftvejene, kan de også smitte som dråbesmitte. De allerede implementerede generelle hygiejniske retningslinjer dækker således alle situationer, hvor der er risiko for smitte med resistente bakterier, både hvad angår smitte fra rask bærer som fra inficerede og mellem såvel personale som patienter. Hvis retningslinjerne ellers efterleves korrekt.
Det er derfor væsentligt altid at overholde de generelle infektionshygiejniske retningslinjer. De vigtigste infektionshygiejniske forholdsregler ved de hyppigst forekommende resistente bakterier i Danmark fremgår af tabel 1.

Hvad kan vi gøre i fremtiden?
Det er forståeligt, at personalet kan blive i tvivl om og urolige for, hvorvidt de i deres kontakt med en patient, som er koloniseret eller inficeret med en resistent eller særlig virulent bakterie, beskytter sig selv og medpatienterne tilstrækkeligt.
De generelle infektionshygiejniske retningslinjer forebygger smitte i alle situationer og mellem såvel patient som personale og den anden vej. De skal derfor være kendt af alle med kontakt til patienter, og efterlevelsen af retningslinjerne skal dagligt tages op til fælles dialog i den tværfaglige personalegruppe.
Efterleves de generelle infektionshygiejniske retningslinjer, er det ikke nødvendigt at udarbejde retningslinjer/vejledninger for hver resistent bakterie, der måtte se dagens lys i fremtiden. Det væsentlige er at have et indgående kendskab til smittevejene, da man herved kan iværksætte supplerende infektionshygiejniske retningslinjer, når dette er nødvendigt for at forebygge smittespredning. som allerede arbejder i sundhedsvæsenet, er derfor meget essentielt. Statens Serum Institut har udviklet tværfaglige undervisningsmaterialer i emnerne håndhygiejne, hygiejne i primærsektoren og forebyggelse af kateterrelaterede urinvejsinfektioner til bl.a. at løfte denne opgave (19).
For at komme problemet med de resistente bakterier til livs er det, ud over efterlevelse af de infektionshygiejniske retningslinjer som beskrevet ovenfor, også nødvendigt at sætte ind på en anden front, nemlig anvendelsen af bredspektrede antibiotika til såvel mennesker som dyr.
Det er meget væsentligt, at der i fremtiden gøres en stor indsats for at nedbringe forbruget af denne type antibiotika. Sundhedsstyrelsen nedsatte derfor, efter beslutning fra Indenrigs- og Sundhedsministeriet, i 2010 et tværfagligt antibiotikaråd, Det Nationale Antibiotikaråd, der skal komme med forslag til løsninger af problemet (5).
En fælles indsats på såvel hygiejne- som antibiotikafronten er vores våben i kampen mod de resistente bakterier, men vi er nødt til at handle hurtigt og effektivt, så vi kan nå at vende udviklingen og hindre, at endnu flere resistente bakterier får fodfæste i Danmark.
Jette Holt
Født 1958, uddannet fra Sygeplejeskolen ved Århus Amtssygehus 1982. Herefter arbejdet på operationsgang i Århus, Grønland og Viborg og senere på ortopædkirurgisk, medicinsk og intensiv afdeling. Sygeplejelærer ved Diakonissestiftelsens Social- og Sundhedsskole og i 1998 hygiejnesygeplejerske ved Den centrale afdeling for sygehushygiejne ved Statens Serum Institut med ansvar for infektionshygiejnisk rådgivning for Grønland, for uddannelse og undervisning og herunder udvikling af e-learning-programmer på nationalt, nordisk og europæisk niveau. SD med speciale i uddannelse og undervisning fra Danmarks Sygeplejerskehøjskole i 1995, specialuddannelse i infektionshygiejne i 2002, ledende auditoruddannelse i 2006, diplomuddannelse i sundhedspædagogik 2000, cand.pæd.pæd. fra Danmarks Pædagogiske Universitet i 2004.
Anne Kjerulf
Født 1962, tog medicinsk embedseksamen fra Københavns Universitet i 1989. Herefter turnus ved Næstved Centralsygehus samt ansættelser på kliniske og klinisk mikrobiologiske afdelinger på Rigshospitalet, Herlev Hospital, Hvidovre Hospital, Statens Serum Institut, og lektor ved Københavns Universitet. Ph.d.-afhandling fra Københavns Universitet i 1998 og speciallæge i klinisk mikrobiologi i 2005. Siden 1. december 2006 afdelingslæge ved Central Enhed for Infektionshygiejne, Statens Serum Institut, hvor hun bl.a. er ansvarlig for udarbejdelse af den nationale desinfektionspolitik.
Jette Holt og Anne Kjerulf er begge ansat i Central Enhed for Infektionshygiejne, Statens Serum Institut.
Litteratur
- Antibiotika; www.ssi.dk > Aktuelt > Temasider > Antibiotika.
- EPI-NYT 47, 2010; www.ssi.dk > Aktuelt > Nyhedsbreve >EPI-NYT> 2010 >Uge 47 – 2010
- DANMAP 2010.
- Frimodt-Møller N, Hammerum AM, Bagger-Skjøt L et al. Global antibiotikaresistensudvikling. Ugeskrifti for Læger 2006;168(36):3008.
- EPI-NYT 1, 2011; www.ssi.dk > Aktuelt > Nyhedsbreve >EPI-NYT> 2010 >
Uge 1 – 2011. - www.ssi.dk > Sygdomsleksikon >M >Methicillin resistente Staphylococcus aureus.
- Sundhedsstyrelsen, Vejledning om forebyggelse af spredning af MRSA, 2006; www.sst.dk > Sundhed og forebyggelse > Smitsomme sygdomme >MRSA > Vejledning om forebyggelse af spredning af MRSA.
- www.ssi.dk > Aktuelt > Temasider > Clostridium difficile.
- EPI-NYT 13, 2009; www.ssi.dk > Aktuelt > Nyhedsbreve >EPI-NYT> 2009 Uge 13 – 2009.
- EPI-NYT 15, 2010; www.ssi.dk > Aktuelt > Nyhedsbreve >EPI-NYT> 2010 >Uge 15 – 2010.
- DANMAP 2009.
- Tham J, Odenholt I, Walder M et al. Extended-spectrum beta-lactamaseproducing Escherichia coli in patients with travellers’diarrhoea. Scand J Infect Dis 2010;42:275-80.
- Tängden T, Cars O, Melhus A, Löwden E. Foreign travel is a major risk factor for colonization with Escherichia coli producing CTX-M-type extendedspectrum beta-lactamases: a prospective study with Swedish volunteers. Antimicrob Agents Chemother 2010;54:3564-8.
- Dancer SJ. The role of environmental cleaning in the control of hospital-acquired infection. J Hosp Infect 73:378-385;2009
- www.ssi.dk > Smitteberedskab > Infektionshygiejne > Undervisning > Værd at vide om håndhygiejne.
- Sundhedsstyrelsen, Vejledning om human immundefekt virus HIV og forebyggelse af blodbåren smitte, 1992.
- Abad C, Fearday A, Safdar N. Adverse effects of isolation in hospitalised patients: a systematic review. J Hosp Infect 76:97-102, 2010
- Nationale infektionshygiejniske retningslinjer om undersøgelse, behandling og pleje af patienter med smitsomme sygdomme, herunder isolation (høringsversion marts 2011; www.ssi.dk > Smitteberedskab > Infektionshygiejne
> Aktuelt > Materialer på vej > Nationale infektionshygiejniske retningslinjer om undersøgelse, behandling og pleje af patienter med smitsomme sygdomme, herunder isolation. - www.ssi.dk > Smitteberedskab>Infektionshygiejne>Undervisning (Interaktiv
undervisning).
Holt J, Kjerulf A. Preventing new, resistant bacteria using old methods. Sygeplejersken 2011;(20):63-9.
Cases of new, particularly virulent types of known bacteria, and the development of resistance in known bacteria, may put staff at risk during everyday clinical activities with patients. In recent years resistant tuberculosis, resistant staphylococci (MRSA, Methicillin Resistant Staphylococcus aureus), resistant intestinal bacteria (e.g. ESBL, Extended Spectrum Beta-Lactamase- producing bacteria) and virulent Clostridium difficile 027, have been reported both nationally and internationally. In an effort to prevent the spread of these bacteria, preventative anti-infection measures as described in the national infection control guidelines, the advice given by the National Unit for Infection Control (Central Enhed for Infektionshygiejne), as well as from the hospitals' or institution's own hygienic-measures or infection-control teams are highlighted. This article describes developments in the appearance of new, resistant bacteria as well as the hygienic infection-control guidelines and associated precautions.
Key words: Antibiotic resistance, infection hygiene, prophylaxis.
1. Hvordan udvikles antibiotikaresistens?
a. Ved anvendelse af smalspektrede antibiotika.
b. Ved anvendelse af bredspektrede antibiotika.
c. Ved et øget forbrug og en uhensigtsmæssig anvendelse af bredspektrede antibiotika.
2. Hvor findes resistente bakterier i Danmark?
a. Udelukkende på sygehusene.
b. Udelukkende ude i samfundet (primærsektoren).
c. Både på sygehusene og ude i samfundet.
3. Hvorfor er resistente bakterier et problem?
a. Det er vanskeligt og omkostningstungt at behandle infektionen.
b. De er forbundet med øget sygelighed og dødelighed.
c. Både a) og b) er korrekt.
4. Hvordan smitter ESBL-producerende bakterier?
a. Via luften
b. Via kontakt med fæces.
c. Via kontakt med organisk materiale (urin, fæces, sårsekret), der indeholder disse bakterier.
5. Hvad vil det sige at være koloniseret?
a. At man er rask smittebærer.
b. At man er smittet, men er i behandling.
c. At man ikke kan videregive smitte.
6. Hvad var anledningen til, at man indførte de procedurerelaterede retningslinjer i Danmark?
a. At man nu kunne vaccinere mod hepatitis B.
b. At hiv-diagnosen var vanskelig at stille.
c. At man skulle nedsætte forbruget af antibiotika.
7. Hvilke værnemidler anvendes til forebyggelse af kontaktsmitte?
a. Handsker.
b. Handsker og forklæde.
c. Briller og maske.
8. Hvornår anvendes de supplerende infektionshygiejniske retningslinjer?
a. Når man vil være helt sikker.
b. Ved dråbe- og luftbåren smitte.
c. Ved luftbåren smitte og ved dråbesmitte og kontaktsmitte, som ikke kun kan forebygges ved de generelle infektionshygiejniske retningslinjer.
Spørgsmål 1: c
Spørgsmål 2: c
Spørgsmål 3: c
Spørgsmål 4: c
Spørgsmål 5: a
Spørgsmål 6: b
Spørgsmål 7: b
Spørgsmål 8: c
