Sygeplejersken
Hepatisk encefalopati - behandling og pleje
Artiklen beskriver symptomer, udredning og behandling af leversygdommen hepatisk encefalopati. En efterfølgende artikel beskriver sygeplejen til denne gruppe patienter.
Sygeplejersken 2014 nr. 9, s. 88-95
Af:
Mette Munk Lauridsen, læge, ph.d.-studerende

Portal hypertension: Tilstand med højt blodtryk i portalvenen. Definitorisk er trykket for højt, når det er over 12 mmHg. Kan opstå, når blodet har svært ved at passere leveren, som det ses ved skrumpelever, hvor leveren er hård og ueftergivelig.
Forgrenede aminosyrer: Kosttilskud i pulverform, der indeholder aminosyrerne valin, leucin og isoleucin. Virker ved at forbedre omsætningen af affaldsstoffer i kroppen og opbygger muskelmasse.
Variser i spiserøret: Åreknuder i spiserøret, der opstår, fordi blodet fra tarmen finder andre veje at løbe i stedet for, som hos normale, at sive igennem leveren, hvor det renses.
Ascites: Væskeansamling i bughulen, som kan optræde ved tilstande med portal hypertension. Behandles med vanddrivende medicin eller ved drænering (paracentese).
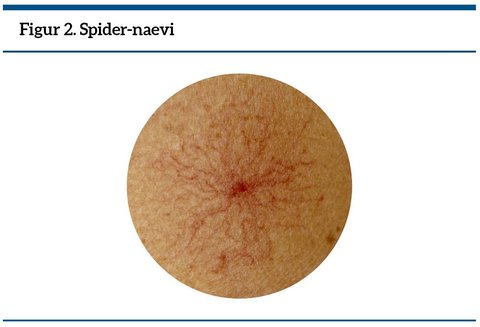
Spider-naevi: Små karudvidelser, som især findes i ansigt og på brystkassen. De forsvinder kortvarigt, når man trykker på dem, og når man slipper, fyldes de med blod fra midten og ud. Finder man mere end 5 spider-naevi hos en patient, skal man mistænke leversygdom, medmindre der er tale om en gravid person.
Ændret hjernefunktion er hyppigt forekommende blandt levercirrosepatienter, og årsagerne er mange, hepatisk encefalopati (HE) er en af dem. HE er en komplikation til leversygdom og er debutsymptom hos 10 pct. af patienterne, som viser sig at have levercirrose, hvilket i sig selv er forbundet med en betydelig mortalitet. Ca. 65 pct. med HE er døde, inden der er gået et år (1). Den høje dødelighed har været uændret igennem de sidste 20 år.
Hepatisk encefalopati kan manifestere sig ved ganske let påvirkning af kognitive funktioner til en dødlignende bevidstløshed. Tilstanden kan give anledning til stor angst og bekymring blandt pårørende og hos os, der er ansvarlige for patientens behandling og pleje. Patienterne har ofte ringe sygdomsindsigt, og det kan være en tung sag at møde dem, men tilgangen lettes, hvis man møder dem med faglighed og viden. Derfor er målet med denne artikel at sætte fokus på hepatisk encefalopati.
Ætiologi
HE er en såkaldt metabolisk encefalopati. Det betyder, at det ikke er hjernen i sig selv, der er syg, men at den lider under, at kroppens homeostase er forstyrret, se boks 1.
Leveren er den største kirtel, vi har i kroppen, og den har en lang række funktioner. Bl.a. er leveren ansvarlig for at afgifte blodet for affaldsstoffer fra tarmen, medicin, alkohol og andre toksiner. Når leveren er syg, bevirker tabet af levercellefunktion og portal hypertension, se boks 1, at affaldsstoffer fra tarmen ikke fjernes fra blodet i tilstrækkelig grad. Det urene blod når hjernen, og her reagerer hjernens støtteceller med at svulme op.
Den metaboliske hjernepåvirkning, som ses ved hepatisk encefalopati, står i modsætning til den organiske hjerneskade, hvor der er skader i selve hjernen. En organisk hjerneskade kunne f.eks. være demens, herunder alkoholdemens, og apopleksi. Kendetegnende for sidstnævnte er, at der oftest vil være ensidige neurologiske udfald f.eks. ensidig lammelse og sensibilitetsforstyrrelser. Herved kan tilstanden ofte skelnes fra HE.
Den vanlige nerveoverledning forstyrres dermed. Ammoniak er et af de affaldsstoffer, der dannes i tarmen. Ammonium er et affaldsstof fra proteinnedbrydningen, og selv om hele årsagen til HE’s opståen ikke er fuldt klarlagt, er man enige om, at ammonium spiller en hovedrolle i udviklingen af HE (2). De symptomer, der kan ses, er resumeret i figur 1 (klik på figuren for at se den i fuld størrelse)
Hvem får hepatisk encefalopati?
Det er en forudsætning for at få HE, at portal hypertension og/eller betydelig nedsat leverfunktion er til stede. De, der ikke har dette, får ikke hepatisk encefalopati. Til gengæld skal man 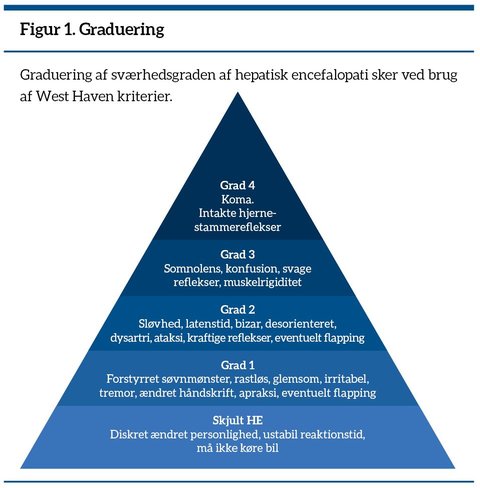
være meget opmærksom på, at der som nævnt er 10 pct., der debuterer med at have en episode med HE og derfor ikke endnu er diagnosticeret med leversygdom, når encefalopatien indtræder. Rigtig mange mennesker går rundt med levercirrose uden at vide det, det giver langt hen ad vejen ikke ret mange symptomer.
Man kan få mistanke om, at en patient har udiagnosticeret levercirrose ved at spørge til alkoholvaner, idet alkohol forårsager over 90 pct. af tilfældene af levercirrose i Danmark. Få input til, hvordan man bedst gør dette i en tidligere udgave af Sygeplejersken (3).
Når man kigger på patienten, kan man se efter såkaldte spider-naevi, se figur 2, (klik på figuren for at se den i fuld størrelse) udtalt rødme i håndfladerne, hvide negle. Finder man > 5 spider-naevi, er det stort set diagnostisk for levercirrose, medmindre der er tale om en gravid kvinde (4).
Kommunikation imellem faggrupper om HE
HE er en hjernepåvirkning, der kan ændre karakter fra time til time, og når det ene vagthold afløser det andet, er vigtigt, at kommunikationen om patientens tilstand er så klar og præcis som muligt. Derfor følger her en kort beskrivelse af, hvordan man kan kategorisere HE. Man kategoriserer først og fremmest patienterne i henhold til årsagen til HE (se boks 2).
Afhængigt af årsagen taler man om tre typer af hepatisk encefalopati:
Type A: Er akut opstået og ses hos patienter med akut leversvigt f.eks. i forbindelse med paracetamolforgiftning.
Type B: Ses hos patienter med cirkulatoriske forstyrrelser, der bevirker, at urent tarmblod ledes udenom leveren f.eks. ved medfødte karanomalier eller portal-vene-trombose, leveren er ikke i sig selv nødvendigvis syg.
Type C: Optræder ved levercirrose, hvor både portal hypertension og nedsat leverfunktion er et problem i vekslende grad.
Dernæst efter sværhedsgraden af den encefalopatiske episode. Man kan give et skøn over sværhedsgraden af HE via West Haven-kriterierne, se figur 1. Slutteligt kategoriseres encefalopatien i henhold til forløbet som enten episodisk, persisterende eller skjult/minimal, se figur 3 og boks 3.
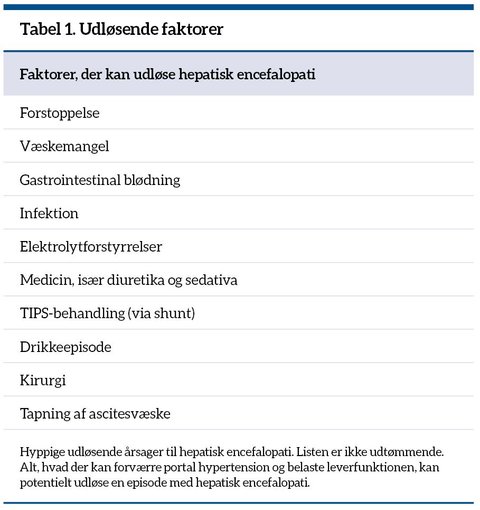
Alle patienter med levercirrose er som udgangspunkt prædisponerede til at udvikle HE, men der er ofte en eller flere udløsende faktorer, som får læsset til at vælte og udløser de enkelte encefalopati-tilfælde. Udløsende faktorer er noget, der enten øger koncentrationen af affaldsstoffer i kroppen eller belaster leverens metaboliske funktion. Det er f.eks. infektioner, væskemangel, nytilkommet medicin, blødning og forstoppelse, se tabel 1, (5).
En ordentlig faglig tilgang til pleje og behandling af patienten med HE indebærer, at man benytter sig af ovennævnte klassifikationer, og at man ved hvert møde med patienten evaluerer fremgang og tilbagegang.
Konsekvenser af HE
Det har store konsekvenser for både patient og pårørende, når HE optræder. Ofte er ingen af parterne klar over, at HE er en mulig komplikation til levercirrose, og det er selvfølgelig et stort chok at opleve et familiemedlem ændre sig fuldstændigt og måske ende med at være i leverkoma, se boks 4. Patienten 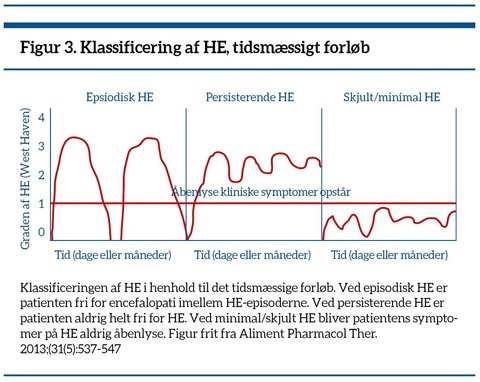
med en mildere grad af HE har høj risiko for faldulykker, de er derudover farlige bilister og har stor risiko for at blive del af et trafikuheld.
Den komatøse patient er helt ubevidst om situationen, men er pga. indlæggelse, sengeleje og levercirrose i stor fare for at pådrage sig hospitalserhvervede infektioner, venetromboser og liggesår. Desuden er der høj risiko for malnutriering og dehydrering, da patienten ikke er i stand til at indtage føde. Det er dog vigtigt at huske på, at patienten oftest kan vågne helt op igen uden varige mén.
Hos patienter med HE er det i udenlandske studier vist, at livskvaliteten er meget ringe sammenlignet med leverpatienter uden HE. Det er især sociale evner, arbejdsevner, seksuel
Man har i løbet af de seneste år tilføjet et ekstra trin i bunden af West Haven skalaen, idet man er blevet opmærksom på, at HE også forekommer i en skjult form (Grad 0). Dvs. at de kognitive forstyrrelser, patienten, eller måske især de pårørende, oplever, ikke kan erkendes via almindelig klinisk undersøgelse og kontakt med patienterne. Den skjulte encefalopati kan have store konsekvenser for patientens livskvalitet og skal diagnosticeres med sensitive psykometriske tests.
funktion og søvnmønster, der påvirkes (6-9). En kæmpe byrde påhviler de pårørende, der skal leve med patienten, som fra dag til dag har vekslende kognitiv funktion (10).
Diagnosticering af HE
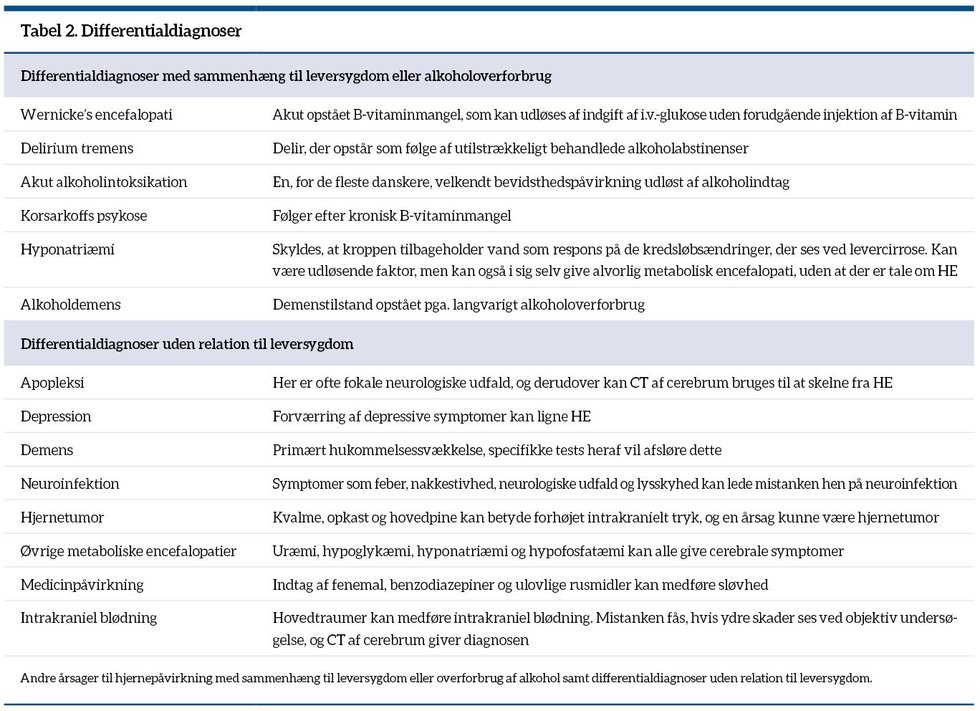
Både hos indlagte patienter med cirrose og patienter i ambulante forløb kan det volde problemer at præcisere, hvad årsagen til kognitive og bevidsthedsmæssige ændringer er. Vigtige differentialdiagnoser er nævnt i tabel 2. Diagnosen hepatisk encefalopati kan stilles, når differentialdiagnoserne er usandsynliggjorte og kun hos en patient med leversygdom. Måling af ammonium i blodet har ingen diagnostisk betydning, men en forhøjet værdi kan støtte diagnosen.
 En førstegangsdiagnose kan derfor kun stilles, når følgende er udført:
En førstegangsdiagnose kan derfor kun stilles, når følgende er udført:
- Grundig anamnese med vægt på medicinoplysninger, tidligere psykiatriske lidelser, kostanamnese samt brug af alkohol og andre rusmidler.
- Objektiv undersøgelse med særlig vægt på neurologisk undersøgelse inkl. undersøgelse for flapping, psykisk vurdering og med angivelse af bevidsthedsniveau ud fra Glascow Coma Scale.
- Blodprøver: levertal, toksikologiprøver herunder s-etanol, infektions- og væsketal, koagulationsstatus med måling af hæmoglobin, trombocytter og koagulationsfaktor II, VII og X, som alle dannes i leveren, desuden albumin, natrium, kalium, magnesium, zink og fosfat.
- Billed-diagnostik: CT-scanning af cerebrum alternativt MR-scanning af cerebrum. Det er ofte også nødvendigt med et røntgenbillede af thorax som led i infektionsudredning.
- Der skal sikres urin- og afføringsprøver og blod til dyrkning.
- Lægen skal udføre diagnostisk ascitespunktur for at undersøge, om der er bakterier i ascitesvæsken (spontan bakteriel peritonitis).
Den skjulte (kaldes minimal eller coverted i udenlandsk litteratur) hepatiske encefalopati er ofte svær at diagnosticere, og man benytter derfor sensitive psykometriske metoder. I Danmark bruger vi kontinuerte reaktionsstidsmålinger, en 10-minutters test, der udføres ved hjælp af en computer. Patienten får høretelefoner på og en håndholdt trykknap i den dominante hånd. Computeren genererer lydstimuli (150 i alt) med vekslende interval på mellem 2-6 sekunder. Patienten skal, straks han registrerer lyden, trykke på trykknappen. Computeren udregner bagefter, hvor stabil man er i sine reaktionstider (11). Er man i stand til at reagere lige hurtigt hver gang, er det godt, men er reaktionstiderne meget vekslende, kan det være tegn på skjult HE.
Internationalt bruges andre tests, og en ordentlig diagnosticering og behandling af skjult HE sker bedst på de sygehusafdelinger, der har erfaring inden for området og kan anvende flere psykometriske metoder.
Man skal være opmærksom på, at leverkoma ikke er en samlet betegnelse for hepatisk encefalopati. Betegnelsen ”leverkoma” skal forbeholdes patienter, der har fuldt udviklet hepatisk encefalopati og er dødlignende bevidstløse.
Case, et eksempel på en sygehistorie
57-årig kvinde indlægges på Fælles Akut Modtageafsnit under diagnosen apoplexia cerebri.
Patientens datter har besøgt hende og fundet hende psykisk ændret og sløv. Hun bliver meget bekymret og aftaler med vagtlægen, at moderen indlægges til vurdering på sygehuset. På sygehuset fortæller datteren til modtagende sygeplejerske, at moderen på det seneste har sovet meget og ved enkelte lejligheder har været aggressiv.
Datteren kan også fortælle, at hendes mor tidligere i livet havde en periode på ca. 11-15 år, hvor hun drak mere end den maksimumsgrænse, der anbefales af Sundhedsstyrelsen. På det seneste har patienten virket sløv og ligeglad, og datteren mistænker, at hun igen drikker for meget alkohol. Moderen har ikke fået særlig meget at spise det seneste stykke tid og bidrager ikke med ret meget til historien.
Ved objektiv vurdering ses kvinden at være fjumret med en smule latenstid og vekslende orientering i tid og sted. Hun mener ikke selv, der er noget i vejen. Kan ikke forstå, hvorfor hun skal indlægges. Der er ingen fokale neurologiske udfald. En mulighed er, at kvinden er dement.
Indlæggelsesblodprøver med levertal viser tegn på kronisk leversygdom, og samtidig ses det, at kvinden ikke har en alkoholpromille. Der er hyponatriæmi og kreatinin i normalområdet, men steget en smule siden sidste blodprøvetagning ved egen læge for tre uger siden. Da var natrium også normal. Der laves en ultralydsscanning, der viser puklet leveroverflade forenelig med levercirrose, og der er en smule ascites. Desuden laves CT-scanning af hjernen uden abnorme fund. Man mistænker nu, at kvinden kan have hjernepåvirkning relateret til leversygdom.
Der iværksættes først og fremmest behandling mod hepatisk encefalopati. Kvindens cerebrale tilstand bedres over de næste par dage. Hun behandles med elektrolytkorrigerende væsketerapi og 10 pct. glukose i.v. samt lakktulose, og der sørges for en ordentlig kost med mange små måltider i løbet af hele dagen og ud på aftenen.
Trods grundig gennemdyrkning fandtes ingen infektion som udløsende årsag. Til gengæld viste det sig, at patienten grundet hævede ben var startet i behandling med vanddrivende medicin (furosemid) for tre uger siden. Dette kan have udløst dehydrering, forstoppelse og belastet leveren yderligere og derved udløst en førstegangsepisode af hepatisk encefalopati.
Leverbiopsi viste efterfølgende en sjælden årsag til levercirrose, nemlig alfa-1-antitrypsinmangel. Kvinden havde op til episoden med encefalopati ikke drukket mere alkohol end vanligt. Fra nu af frarådes hun al indtag af alkohol for at skåne leveren mest muligt. Samtidig seponeres al medicin, der ikke er strengt nødvendigt. Hun udskrives med lakktulose og kommer til ambulant opfølgning efter to måneder, hvor psykometriske tests vil blive udført.
Behandling af HE
Find den udløsende årsag
Det er vigtigt at holde sig for øje, at en patient med HE er en meget skrøbelig patient, som kræver tæt observation og en behandling, der foregriber det kliniske forløb.
Der er en række livstruende årsager til, at HE kan optræde eller forværres. Kan en årsag findes og behandles adækvat, vil komaen ofte lette i løbet af i gennemsnit fire dage. HE er altså, trods den ringe langtidsprognose, en reversibel tilstand og ikke nødvendigvis stoppestedet inden døden. Det er derfor helt afgørende at udrede årsagen. De hyppigste udløsende årsager er listet i tabel 1.
Tidlig enteral ernæring
Tidlig ernæringsterapi til HE-patienter er en af hjørnestenene i behandlingen af den indlagte patient. Det første døgn kan man klare sig med rehydrerende og elektrolytkorrigerende væsketerapi, og i fald patienten ikke indtager føde, kan det være en god idé at give intravenøs glukose forudgået af injektion med B-vitaminer. Dybt komatøse patienter kan selvfølgelig ikke ernæres enteralt (via sonde eller spise selv), risikoen for at aspirere mad til lungerne er alt for stor. De må ernæres med parenteral ernæring efter det første døgn, indtil de er i stand til at forsvare deres luftveje.
Enteral ernæring skal startes så snart som muligt, og det er tilrådeligt, at der udføres en diætistisk vurdering tidligt i forløbet. Patienten skal ikke have proteinfattig kost, men 1,3 g protein/kg/døgn, og kalorieindtaget børe være ca. 35-40 kcal/kg/døgn. Læs mere om ernæringsterapi til leverpatienter på ESPEN Guidelines (www.espen.org).
Medicinsk behandling
Hovedhjørnestenen i den medicinske behandling af hepatisk encefalopati er laktulose, som ved de lettere grader af HE drikkes, men må gives i ventrikelsonde hos den somnolente patient. De fleste steder anbefaler man, at der gives laktulose 20-80 ml/døgn fordelt på doser a 25 ml med 2-4 timers mellemrum, indtil der opnås 3-4 afføringer pr. døgn.
Laktulose kan også gives rektalt hos de dybt komatøse, hvor der er risiko for aspiration ved enteral indgift. Rationalet i brugen af laktulose er dels den direkte udrensende effekt, men laktulose ændrer også pH i afføringen, sådan at dannelsen af ammoniak i tarmen begrænses. Laktulosebehandlingen skal fortsættes efter udskrivelsen, og det er en god idé at udføre en psykometrisk test inden da. Denne test kan gentages, når patienten kommer til ambulant opfølgning, og give et mål for, om der er fremgang i den cerebrale funktion.
Oplever patienten recidiv af HE trods behandling med laktulose, kan tillægges et kosttilskud i form af forgrenede aminosyrer (Bramino®) eller rifaximin, som er et antibiotikum, der har effekt i tarmen og stort set ikke optages til blodet. Rifaximin er meget dyrt, og der er kun evidens for at bruge det i behandlingen af recidiverende HE. For mere information se f.eks. behandlingsinstruksen e-dok.rm.dk, som er det senest opdaterede (12). I tabel 3 er den medicinske behandling resumeret.
Behandling af skjult HE
Skjult HE (West Haven grad 0) findes med psykometriske tests hos ca. halvdelen af danske patienter med levercirrose. Halvdelen af dem, der har skjult HE, vil senere få en episode med åbenlys HE, de har desuden høj risiko for faldulykker, involvering i trafikulykker og er ofte så dårligt fungerende, at det påvirker deres arbejdsevne og sociale liv i ødelæggende grad. Der er derfor også god grund til at finde og forsøge at behandle disse patienter.
Sygeplejersker bliver stadigt mere og mere involveret i især ambulant udredning og behandling af patienter med levercirrose. Sygeplejersker varetager flere steder både fibrosescanning af leveren, udførelse af psykometriske tests til diagnosticering af skjult HE samt livsstilssamtaler, der hjælper patienten med at takle ernærings-, misbrugs- og sociale problemer. På Bispebjerg Hospital er man meget langt fremme i den ambulante tværfaglige behandling og med gode resultater. Man kan læse om deres erfaringer og gode resultater i Ugeskrift for Læger (13).
Hermed er læseren opdateret på den viden, vi har omkring hepatisk encefalopati. Megen ny viden er kommet til de seneste år, og forskningen inden for området er i rivende udvikling. Danmark er en af de nationer, der globalt set er med helt fremme i HE-forskning. Som det fremgår, er det en tilstand, som kan være kompleks, især når der er flere årsager til leverpatientens hjernepåvirkning, store sociale og psykiske problemer, og måske også udfordringer med patientens vilje og evne til at tage medicin som foreskrevet.
I de fleste tilfælde er sagen dog ret ligetil. Patienter, og især pårørende, er glade for, at der spørges ind til psykiske og adfærdsmæssige ændringer. Mange, både pårørende og sundhedspersonale, har måske tidligere været af den opfattelse, at en patient med leversygdom og hjernepåvirkning nok har ”drukket hjernen ud”. Den holdning skal vi til livs, og alle patienter, der får stillet diagnosen levercirrose, bør undersøges for HE og tilbydes behandling ved mistanke herom.
Mette Munk Lauridsen, læge og ph.d.-studerende, Medicinsk Gastroenterologi og Hepatologi, Sydvestjysk Sygehus Esbjerg og OUH.
Læs også artiklen ”Sygepleje til patienter med hepatisk encefalopati” i samme nummer af Sygeplejersken.
Litteratur
- Jepsen P, Andersen PK, Sørensen HT, Vilstrup H. The clinical course of alcoholic cirrhosis with ascites: Effects of liver and kidney function, hyponatremia, and alcohol. Hepatology. 2010;52:896A.
- Dam G, Keiding S, Munk OL, Ott P, Vilstrup H, Bak LK, et al. Hepatic encephalopathy is associated with decreased cerebral oxygen metabolism and blood flow, not increased ammonia uptake. Hepatology. 2012.
- Lauridsen MM. Observation og behandling af alkohol abstinenser. Sygeplejersken. 2009:36-40.
- Schaffalitzky de Muckadell OB, Haunsø S, Vilstrup H. Medicinsk Kompendium. ed: Nyt Nordisk Forlag; 2013.
- Wright G, Chattree A, Jalan R. Management of hepatic encephalopathy. Int J Hepatol. 2011;2011:841407.
- Schomerus H, Hamster W. Quality of life in cirrhotics with minimal hepatic encephalopathy. Metab Brain Dis. 2001;16(1-2):37-41.
- Marchesini G, Bianchi G, Amodio P, Salerno F, Merli M, Panella C et al. Factors associated with poor health-related quality of life of patients with cirrhosis. Gastroenterology. 2001;120(1):170-8.
- Cordoba J, Cabrera J, Lataif L, Penev P, Zee P, Blei AT. High prevalence of sleep disturbance in cirrhosis. Hepatology. 1998;27(2):339-45.
- Groeneweg M, Quero JC, De Bruijn I, Hartmann IJ, Essink-bot ML, Hop WC et al. Subclinical hepatic encephalopathy impairs daily functioning. Hepatology. 1998;28(1):45-9.
- Bajaj JS, Wade JB, Gibson DP, Heuman DM, Thacker LR, Sterling RK et al. The multi-dimensional burden of cirrhosis and hepatic encephalopathy on patients and caregivers. Am J Gastroenterol. 2011;106(9):1646-53.
- Lauridsen MM, Thiele M, Kimer N, Vilstrup H. The continuous reaction times method for diagnosing, grading, and monitoring minimal/covert hepatic encephalopathy. Metab Brain Dis. 2013.
- Vilstrup H. Hepatisk encephalopati: Diagnostik og behandling: Region Midtjylland; 2013. Available from: e-dok.rm.dk
- Andersen MM, Aunt S, Jensen NM, Homann C, Manniche J, Svendsen S et al. Rehabilitation for cirrhotic patients discharged after hepatic encephalopathy improves survival. Danish medical journal. 2013;60(8):A4683.
Lauridsen MM. Hepatic encephalopathy: Treatment and care. Sygeplejersken 2014;(9):88-95.
Hepatic encephalopathy (HE) is a condition in which the brain is affected by liver disease. The condition is a frequent complication of cirrhosis of the liver and is associated with a very poor prognosis. HE occurs because the blood-borne waste is not metabolised in the liver to the same extent as in healthy people. The waste products, especially ammonia, disrupt nerve conduction in the brain. Many patients and their families are not aware that failing brain function and liver cirrhosis are related, and therefore medical knowledge and thorough communication is important when meeting these patients. The condition can be classified by its triggering cause, severity and course. Diagnosis can be quite challenging and often must be based on a comprehensive assessment once other likely causes have been ruled out. There is a disguised form of hepatic encephalopathy which strikes 50 per cent of patients with liver cirrhosis and which cannot be determined by general objective evaluation. The condition impairs quality of life and increases the risk of falls and accidents; and 50 per cent of patients will progress to overt HE. The hidden encephalopathy is diagnosed using continuous response measurements at a highly specialised hospital department. The treatment of hepatic encephalopathy primarily uses fluid therapy and nutrition therapy, as well as lactulose, which reduces the amount of ammonia produced in the intestines. But first and foremost, the encephalopathy episode’s precipitating causes must be identified. Most often constipation, infection, bleeding from varices, or dehydration causes the encephalopathy. Thorough nursing care to these patients is paramount, and good patient care can be ensured by an understanding of the disease among all professions and good communication with patients and relatives.
Keywords: Hepatic encephalopathy, liver cirrhosis, continuous response measurements.
